Neurobiología de Circuitos y Trastornos Psiquiátricos
Neurobiology of Circuits and Psychiatric Disorders
Dr. Mariano Soiza Reilly
JEFE DE GRUPO / Team Leader
Investigador Independiente CONICET
Jefe de Trabajos Prácticos DFBMC-FCEN-UBA
msoizareilly@fbmc.fcen.uba.ar![]() @MSoizaReilly
@MSoizaReilly ![]() @soizareillylab
@soizareillylab
Las enfermedades psiquiátricas como la depresión, la ansiedad y la vulnerabilidad al estrés representan unas de las condiciones mentales más incapacitantes para la vida de los seres humanos. Recientes estudios sugieren que muchos aspectos de dichas patologías podrían tener un origen temprano durante la infancia de los individuos. Nuestro grupo está interesado en entender los mecanismos por los cuales modificaciones en la formación y maduración de circuitos cerebrales durante distintas etapas del neurodesarrollo pueden contribuir a la etiología temprana de enfermedades psiquiátricas.
Psychiatric disorders including depression, anxiety and stress vulnerability represent one of the main disabling conditions for individual’s life. Recent studies suggest that many aspects of these pathologies could have an early origin during childhood. Our team is interested in understanding how maladaptive neurodevelopmental mechanisms engaged in the maturation of neural circuits could contribute to the early etiology of psychiatric disorders.
Para comprender el origen temprano de enfermedades psiquiátricas como la ansiedad o la depresión utilizamos el ratón como modelo experimental, empleando un abordaje integral que incluye el uso de anatomía sináptica de alta resolución y distintas herramientas genéticas y fisiológicas, que nos permiten estudiar tanto la arquitectura de los circuitos cerebrales como así también su funcionalidad.
Early origins of Anxiety and Depression
To understand the early origins of psychiatric disorders including anxiety and depression we apply a multidisciplinary approach that includes high-resolution synaptic anatomy and novel genetic and physiological tools that allow us to explore the architecture and function of brain circuits in mice.
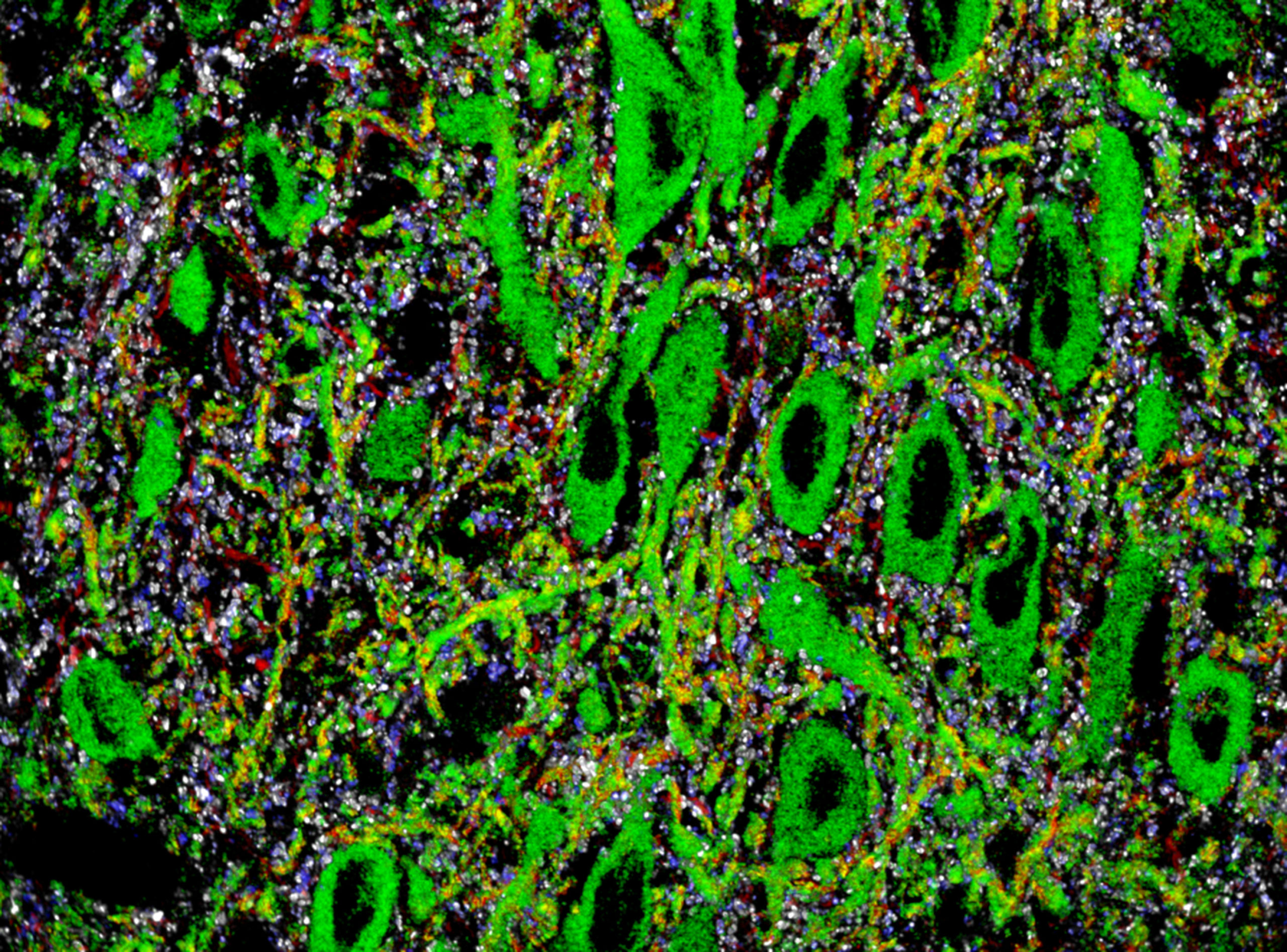
En nuestro laboratorio empleamos una técnica microscópica de fluorescencia de alta resolución denominada Array Tomography (AT). AT permite evaluar cuantitativamente la organización espacial y la arquitectura fina de los circuitos sinápticos presentes en el sistema nervioso. Dicho abordaje resulta de gran utilidad para investigar la presencia de cambios estructurales en los circuitos neurales que puedan contribuir a la fisiopatología de trastornos mentales. Nuestro lab forma parte de la red internacional “Array Tomography Training and Network” financiada por la Chan Zuckerberg Initiative, EEUU.
Exploring Synaptic Circuits with Array Tomography
In the lab we apply a high-resolution fluorescence microscopy technique called Array Tomography (AT). AT allows quantitative interrogation about the spatial organization and fine architecture of synaptic circuits present in the nervous system. This approach enables to investigate very precisely how structural changes in neural circuits could contribute to the pathophysiology of mental illnesses. Our lab is part of an international network “Array Tomography Training and Network” funded by the Chan Zuckerberg Initiative, USA.
- Patricia Gaspar (Institut du Cerveau et de la Moelle épinière, Francia)
- Flavia Saravia (IBYME-CONICET – FCEN, UBA, Argentina)
- Jacques Barik y Sebastián P. Fernández (Institut de Pharmacologie Moléculaire et Cellulaire – CNRS – Univ. Côte D’Azur, Francia)
- Marco Diana y Eric Schwartz (Saints-Pères Paris Institute for the Neurosciences – CNRS – Univ. Paris Cité, Francia)
- Francisco J. Urbano y Paula Perissinotti (IFIBYNE – FCEN, UBA – CONICET, Argentina)
- Elena Avale (INGEBI – CONICET, Argentina)
– FACAL, C.L., PAEZ-PAZ, I., PEREYRA, A.E., GAGUINE, C., CLERICI-DELVILLE, R., FOLTRAN, R., SOIZA-REILLY, M., AVALE, M.E. Artificial microRNAs targeting Tau enable post-symptomatic functional recovery in aged tauopathy mice. MOL THER NUCLEIC ACIDS; Lugar: CAMBRIDGE; Año: 2026 vol. 37(1):102843. 10.1016/j.omtn.2026.102843.
– CAMPOS, R.C., MARTI, F., RIGONI, D., FOFO, H., POUSINHA, P., ORTIZ, V., ROYON, L., VIOLAIN, M., HECK, N., FAURE, P., SOIZA-REILLY, M., FERNANDEZ, S.P., BARIK, J. Nicotine disrupts top down habenular control over cholinergic inputs to the ventral tegmental area to increase motivational valence of food rewards. BIOL PSYCHIATRY; Lugar: NEW YORK; Año: 2026 vol. 99(6):492-505. doi: 10.1016/j.biopsych.2025.06.036.
– CONTESSE, T.; GOMES-RIBEIRO, J.; ROYON, L.; FOFO, H.; BRAINE, A.; GLANGETAS, C.; ZHANG, S; BARBANO, M. F.; SOIZA-REILLY M.; GEORGES, F.; BARIK, J.; FERNANDEZ, S.P. Social stress increases anxiety by GluA1-dependent synaptic strengthening of ventral tegmental area inputs to the basolateral amygdala. BIOLOGICAL PSYCHIATRY; Lugar: NEW YORK; Año: 2025 vol. 98(10):788-801. doi: 10.1016/j.biopsych.2025.04.007.
– FACAL C.L., FERNANDEZ BESSONE I., MUÑIZ J.A., PEREYRA A.E., PEDRONCINI O., PÁEZ-PAZ I., CLERICI-DELVILLE R., ARNAIZ C., URRUTIA L., FALASCO G., ARGAÑARAZ C.V., SAEZ T., MARIN-BURGIN A., SOIZA-REILLY M., FALZONE T., AVALE M.E. Tau reduction with artificial microRNAs modulates neuronal physiology and improves tauopathy phenotypes in mice MOL THER.; Lugar: Cambridge (USA); Año: 2024 vol. 32(4), p 1080 – 1095.
- ICGEB CRP 2024 Grant, Trieste, Italy.
- IBRO CRG 2024 Grant, IBRO.
- CZI Grant Advancing Imaging Through Collaborative Projects: Array tomography Training and Network, Chan Zuckerberg Initiative, EEUU.
- Subsidio ECOS-Sud 2022, Ministerio de Ciencia, Tecnología e Innovación, Argentina – Ministère de l’Enseignement Supérieur et de la Recherche, Francia.
- Subsidio para la Investigación en Cs. Biomédicas 2022, Fundación Florencio Fiorini – Academia Nacional de Medicina.
- Subsidio PIP-2021-2023, CONICET.
- Subsidio PICT-2019 D, Agencia I+D+i.
- 2019 Young IBRO Connecting Award, IBRO.
- 2018 Return Home Grant, International Society for Neurochemistry.
- 2017 IBRO Return Home Award.
Lab meeting at The Node – The Company of Biologists
Lab meeting with the Soiza-Reilly lab
Emociones: de roedores a humanos.
A Todo Neuro, Podcast de la Sociedad Argentina de Investigación en Neurociencias
Niños estresados, ¿adultos vulnerables?
por Magalí de Diego (CTyS-UNLaM)
Investigan cómo impacta sufrir estrés durante la infancia
por Magalí de Diego (CTyS-UNLaM)
por Bruno Geller (CONICET)
The people behind the papers – Carla Argañaraz, Tamara Adjimann and Mariano Soiza-Reilly
por la revista DEVELOPMENT
Integrantes del grupo / Team members

Rocío Foltran
Becaria Posdoc CONICET


Carla Argañaraz
Becaria Doctoral CONICET


Tadeo Riccetti
Estudiante de Lic. Biología

Tadeo Riccetti
Estudiante de Lic. Biología

Milagros Albarrán
Estudiante de Lic. Biología

Milagros Albarrán
Estudiante de Lic. Biología

Grace Wu
Becaria Doctoral CONICET


Melina Maidana
Becaria Doctoral CONICET


Máximo Camacho
Estudiante de Lic. Biología

Máximo Camacho
Estudiante de Lic. Biología